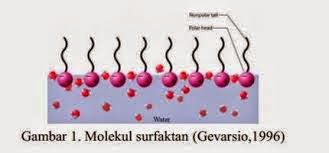
A. Pengertian dan Sifat Surfaktan
Surfaktan adalah suatu zat yang
mempunyai kemampuan untuk menurunkan tegangan permukaan (surface tension) suatu medium dan menurunkan tegangan antarmuka (interfacial tension) antar dua fase yang
berbeda derajat polaritasnya. Istilah antarmuka menunjuk pada sisi antara dua
fase yang tidak saling melarutkan, sedangkan istilah permukaan menunjuk pada
antarmuka dimana salah satu fasenya berupa udara (gas) (Rosen 2004).
Struktur surfaktan dapat digambarkan
seperti berudu yang memiliki kepala dan ekor. Bagian kepala pada surfaktan
bersifat hidrofilik atau polar dan kompatibel dengan air, sedangkan bagian ekor
bersifat hidrofobik atau non-polar dan lebih tertarik ke minyak/lemak. Bagian
kepala pada surfaktan ini dapat bersifat anionik, kationik, amfoterik atau nonionik,
sedangkan bagian ekor dapat berupa hidrokarbon rantai linier atau cabang.
Konfigurasi kepala-ekor tersebut membuat surfaktan memiliki fungsi yang beragam
di industri (Hui 1996; Hasenhuettl 1997).
B. Klasifikasi Surfaktan
Berdasarkan muatan ion pada
gugus hidrofiliknya, surfaktan dikelompokkan menjadi 4 kelompok, yaitu
surfaktan anionik, kationik, amfoterik dan nonionik.
a. Surfaktan Anionik
Surfaktan anionik bermuatan negatif
pada bagian hidrofiliknya. Aplikasi utama dari surfaktan anionik yaitu untuk
deterjensi, pembusaan dan emulsifier pada produk-produk perawatan diri
(personal care product), detergen dan sabun. Kelemahan surfaktan anionik adalah
sensitif terhadap adanya mineral dan perubahan PH. Contoh surfaktan anionik,
yaitu linier alkilbenzen sulfonat, alkohol sulfat, alkohol eter sulfat, metil
ester sulfonal (MES), fatty alkohol eter fosfat.
b. Surfaktan Kationik
Surfaktan kationik bermuatan
positif pada bagian hidrofiliknya. Surfaktan kationik banyak digunakan sebagai
bahan antikorosi, antistatik, flotation
collector, pelunak kain, kondisioner, dan bakterisida. Kelemahan surfaktan
jenis ini adalah tidak memiliki kemampuan deterjensi bila diformulasikan ke
dalam larutan alkali. Contoh surfaktan kationik, yaitu fatty amina, fatty
amidoamina, fatty diamina, fatty amina oksida, tertiari amina etoksilat,
dimetil alkil amina dan dialkil metil amina.
c. Surfaktan Nonionik
Surfaktan nonionik tidak memiliki muatan, tetapi mengandung grup yang
memiliki afinitas tinggi terhadap air yang disebabkan adanya interaksi kuat
dipol-dipol yang timbul akibat ikatan hidrogen. Aplikasi surfaktan nonionik umumnya
pada detergen untuk suhu rendah dan sebagai emulsifier. Keunggulan surfaktan
ini adalah tidak terpengaruh oleh adanya air sadah dan perubahan pH. Contoh
surfaktan nonionik adalah dietanolamida, alkohol etoksilat, sukrosa ester,
fatty alkohol poliglikol eter, gliserol monostearat, sukrosa distearat,
sorbitan monostearat, sorbitan monooleat, gliserol monooleat dan propilen
glikol monostearat.
d. Surfaktan Amfoterik
Surfaktan amfoterik memiliki
gugus positif dan negatif pada molekul yang sama sehingga rantai hidrofobik
diikat oleh bagian hidrofilik yang mengandung gugus positif dan negatif.
Surfaktan amfoterik sangat dipengaruhi oleh perubahan pH, dimana pada pH rendah
berubah menjadi surfaktan kationik dan pada pH tinggi akan berubah menjadi
surfaktan anionik. Surfaktan jenis ini umumnya diaplikasikan pada produk sampo
dan kosmetik. Contohnya adalah fosfatidilkolin (PC), fosfatidiletanolamina
(PE), lesitin, asam aminokarboksilat dan alkil betain.
C. Karakteristik Surfaktan
1. HLB (Hydrophile-Lipophile
Balance)
HLB merupakan suatu parameter
untuk mengkorelasikan secara kuantitatif struktur surfaktan dengan aktifitas
permukaannya. Secara formal, harga HLB diberikan dalam kisaran skala 0-20.
Semakin tinggi nilai HLB menunjukkan surfaktan makin bersifat hidrofilik
sehingga lebih mudah larut dalam air dan pada umumnya digunakan sebagai bahan
pelarut (solubilizing agents) yang
baik, detergen, dan penstabil untuk emulsi O/W. Sementara bila nilai HLB
semakin rendah menunjukkan kelarutan dalam air yang rendah sehingga sering
digunakan sebagai pelarut air dalam minyak dan penstabil emulsi W/O yang baik
(Myers 2006).
2. Tegangan Permukaan
Tegangan permukaan dirumuskan
sebagai energi yang dibutuhkan untuk memperbesar permukaan suatu cairan sebesar
1 cm2. Tegangan permukaan disebabkan oleh adanya gaya tarik-menarik
dari molekul cairan. Semakin besar ikatan antar molekul-molekul dalam cairan,
semakin besar tegangan permukaannya (Bodner dan Pardue 1989).
Surfaktan dapat diserap pada
permukaan atau antarmuka dengan bagian hidrofiliknya berorientasi pada fase
yang lebih rendah viskositasnya dan bagian hidrofobiknya berorientasi pada uap
atau fase yang kurang polar. Berbagai jenis surfaktan memiliki kemampuan yang
berbeda untuk mengurangi tegangan permukaan atau tegangan antarmuka karena
struktur kimia yang berbeda.
3. Tegangan Antarmuka
Tegangan antarmuka adalah gaya
persatuan panjang yang terjadi pada antarmuka dua fase cair yang tidak dapat
bercampur. Surfaktan berfungsi sebagai senyawa aktif yang dapat digunakan untuk
menurunkan energi antarmuka yang membatasi dua cairan yang tidak saling larut.
Kemampuan ini disebabkan oleh gugus hidrofilik dan hidrofobik yang dimilki oleh
surfaktan. Surfaktan akan menurunkan gaya kohesi dan sebaliknya meningkatkan
gaya adhesi sehingga dapat menurunkan tegangan antarmuka (Matheson 1996).
Tegangan antarmuka sebanding dengan tegangan permukaan, tetapi nilai tegangan
antarmuka akan selalu lebih kecil daripada tegangan permukaan pada konsentrasi
yang sama (Moecthar 1989).
4. Kemampuan Pembusaan
Kebanyakan surfaktan dalam
larutan dapat membentuk busa, baik diinginkan maupun tidak diinginkan dalam
penggunaanya. Kestabilan busa diperoleh dari adanya zat pembusa (surfaktan).
Zat pembusa ini teradsorpsi ke daerah antarfase dan mengikat
gelembung-gelembung gas sehingga diperoleh suatu kestabilan (Ware et al. 2007). Kemampuan pembusaan
surfaktan dipengaruhi oleh panjang rantai hidrokarbon. Dibandingkan dengan
surfaktan anionik sebagai agen pembusa yang telah lama digunakan, surfaktan nonionik
dianggap sebagai surfaktan yang memiliki kemapuan pembusaan yang lebih rendah.
5. Stabilitas Emulsi
Stabilitas emulsi merupakan
keseimbangan antara gaya tarik-menarik dan gaya tolak-menolak yang terjadi
antar partikel dalam sistem emulsi. Jika kedua gaya tersebut dipertahankan
tetap seimbang, maka partikel-partikel dalam sistem emulsi akan dapat
dipertahankan untuk tidak bergabung. Mekanisme kerja dari surfaktan untuk
menstabilkan emulsi yaitu dengan menurunkan tegangan permukaan dan membentuk
lapisan pelindung yang menyelimuti globula fase terdispersi sehingga senyawa
yang tidak larut akan lebih mudah terdispersi dalam sistem dan menjadi stabil. Gugus hidrofilik dan lipofilik
yang dimiliki surfaktan dapat membentuk lapisan film pada bagian antarmuka dua
cairan yang berbeda fase. Adanya dua gugus tersebut pada emulsifier
memungkinkan emulsifier membentuk selaput tipis atau disebut juga dengan
lapisan film, disekeliling globula-globula fase terdispersi dan bagian luarnya
berikatan dengan medium pendispersi (Suryani et al. 2000). Pembentukan film tersebut mengakibatkan turunnya
tegangan permukaan kedua cairan yang berbeda fase tersebut sehingga
mengakibatkan turunnya tegangan antarmuka.
6. pH
Derajat
keasaman (pH) merupakan salah satu karakteristik surfaktan. Setiap jenis
surfaktan memiliki pH yang berbeda-beda, misalnya saja pH dari surfaktan
dietanolamida berkisar antara 9 dan 10. Dalam penggunaan surfaktan, pH perlu
diperhatikan karena akan berpengaruh terhadap aktivitas surfaktan tersebut
meskipun ada sebagian jenis surfaktan yang tidak dipengaruhi oleh perubahan pH.